동구토토 꽁머니 지급 '구세정'·씨티씨 '원투정', 클로미프라민+실데나필 복합제
암젠, '임델트라+임핀지' 병용투여 소세포폐암 대상 3상 승인
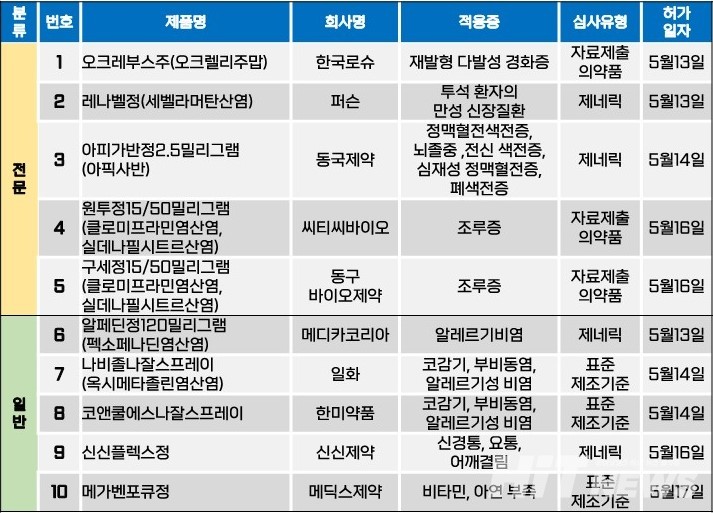
지난주(5월 13일~5월17일) 총 10개 품목이 식품의약품안전처로부터 품목허가를 받았다. 전문의약품 및 일반의약품 모두 각 5개 품목 씩이다. 이들은 다발성 경화증, 만성 신장질환, 색전증, 뇌졸중, 조루증 등 다양한 적응증으로 허가됐다.
동구토토 꽁머니 지급제약과 씨티씨토토 꽁머니 지급가 공동 개발한 조루증 치료 복합제가 지난 16일 허가됐다.
동구토토 꽁머니 지급제약의 ‘구세정’과 씨티씨토토 꽁머니 지급의 ‘원투정’은 조루증 치료제 ‘클로미프라민’과 발기부전 치료제 ‘실데나필’을 주성분으로하는 복합제로, 각 15mg, 50mg 용량을 포함하고 있다.
동구토토 꽁머니 지급제약 측에 따르면, 이 제품들은 컨덴시아정(성분 클로미프라민) 및 비아그라정(성분 실데나필) 등 기존 치료제들에 비해 ‘질내 삽입 후 사정까지의 시간(IELT)’을 개선했다. 구세정은 투약 후 4주 시점에서부터 컨덴시아정 대비 1.46±0.40분, 비아그라정 대비 1.85±0.39분 유의하게 IELT를 증대시켰다.
또한 ‘환자자기결과 평가(PRO, Patient Reported Outcomes)’ 결과, 유효성 및 안전성 측면에서 대조군들과 견줄 정도로 양호하며, 치료군 간 차이가 유의함을 확인한 것으로 나타났다.
동구토토 꽁머니 지급제약 관계자는 “씨티씨토토 꽁머니 지급의 다양한 개량 신약 복합제 개발 경험과 비뇨의학과을 주력으로 한 동구토토 꽁머니 지급제약의 영업력이 만나 개량신약 도입이 주춤했던 비뇨기 시장에서 상당한 시너지를 가져올 수 있을 것으로 기대한다”고 설명했다.
양사는 현재 사업제휴 계약 체결 후 제품 생산 준비를 마친 상태다. 제품 출시 시기를 앞당기기 위해 공장 시생산 등 마무리 과정에 박차를 가하겠다는 입장이다. 또, 복합제 출시 후 PMS(시판후조사)를 활용해 시장 선점 효과를 누림과 동시에 국내 임상자료를 인정하는 지역을 대상으로 허가를 진행할 예정이며, 유럽과 미국 등 추가적인 인종간 개체 차 시험을 통해 추후 허가를 진행할 계획이다.
조용준 동구토토 꽁머니 지급제약 대표는 “1970년대 국내 최초 전립선비대증 치료제인 쎄닐톤을 출시한 이후, 유로파서방정, 탐스로신 등 비뇨기 대표품목으로 사업을 확대하고 있다”며 “이번 조루 복합치료제를 통해 급속히 확대되고 있는 비뇨기 시장에 공격적인 마케팅을 펼쳐 국내 비뇨의학과 처방 1위 회사로 나아갈 뿐 아니라 해외시장 진출의 교두보로 삼을 것”이라고 밝혔다
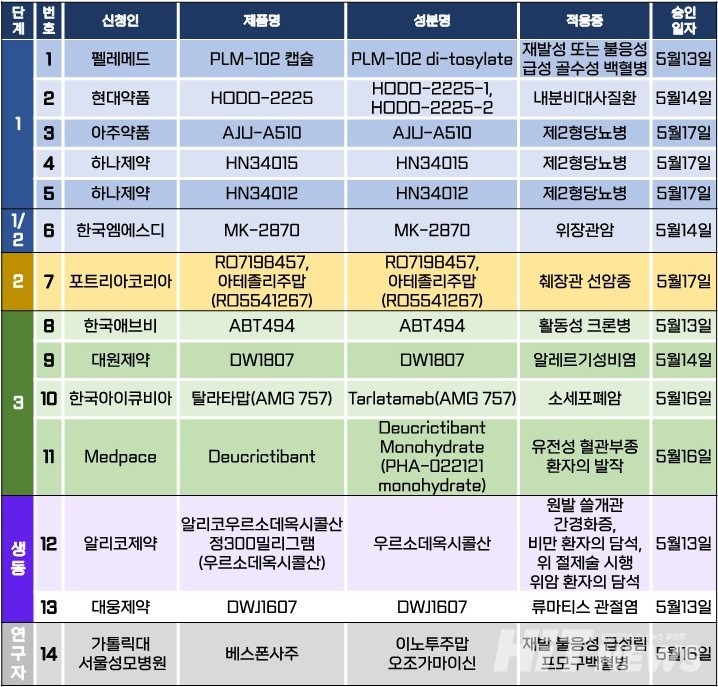
임상시험계획은 총 14건이 승인됐다. 세부적으로 △1상 5건 △1/2상 1건 △2상 1건 △3상 4건 △생물학적 동등성 2건 △연구자임상 1건 등이다. 이 임상시험들은 제2형당뇨병, 활동성 크론병, 알레르기성비염 등 질환과 급성 골수성 백혈병, 위장관암, 췌장관선암종, 소세포폐암 등 암종을 대상으로 승인됐다.
암젠이 개발중인 소세포폐암 치료제 ‘임델트라(성분 탈라타맙)’의 3상 임상시험계획이 지난 16일 승인됐다.
임델트라는 소세포폐암 환자에서 발현되는 'DLL3(델타-유사 리간드 3)'단백질과 면역세포 및 T세포 발현과 관련된 'CD3'단백질을 타깃하는 이중특이항체다.이중특이항체는 두 개의 단일클론항체를 혼합 사용한 것 보다 유리할 수 있어 종양 면역 요법, 자가 면역 질환 분야 등에서 치료제 개발에 다양하게 활용되고 있다.
이번 임상은 백금, 에토포시드 및 더발루맙(제품명 임핀지) 투약 이후 확장 병기 소세포폐암(ES-SCLC)이 있는 환자에서 ‘임델트라+더발루맙’ 병용 요법 대 더발루맙 단독 요법을 비교하는 라벨 공개, 다기관, 무작위 배정 3상 연구(연구명 DeLLphi-305)다.
연구진은 24명(글로벌 550명) 확장 병기 소세포폐암 환자를 대상으로, 2028년 9월까지 △서울대병원 △서울아산병원 △분당서울대병원 △국립암센터 △연세대 의대 세브란스병원 △삼성서울병원 등 의료기관에서 임상시험을 진행할 예정이다.
연구진은 일차유효성평가변수를 전체생존기간(OS)으로 설정했으며, 주요 이차유효성평가변수는 무진행생존기간(PFS)로 정했다.
한편, 미국 FDA는 지난 16일(현지시간) 임델트라를 백금 기반 항암화학요법 치료를 진행 중이거나 실패한 확장 병기 소세포폐암 환자를 위한 치료제 가속 승인했다. 이 허가의 주요 연구는 17개국 56개 의료기관에서 220명의 환자를 대상으로 진행된 2상 임상인 ‘DeLLphi-301’이다.
연구 결과 임델트라 10mg을 2주 간격으로 투여한 환자 99명의 객관적반응률(ORR)은 40%(95% CI: 31-51)였으며, 반응기간(DoR) 중앙값은 9.7개월(95% CI : 2.7-20.7)로 나타났다. 전체생존기간 중앙값은 14.3개월이었으며, 아직 데이터가 성숙하지 않은 상태다.
환자들 사이에서 보고된 이상반응은 사이토카인방출증후군(CRS, 55%), 피로(51%), 발열(36%), 미각이상(36%), 식욕 감소(34%), 근골격계 통증(30%), 변비(30%), 빈혈(27%), 메스꺼움(22%) 등 순이었다. 치료 관련 이상반응(TEAE)으로 인한 영구 중단은 7%였으며, 주로 1차 및 2차 용량 증량에 의한 CRS가 원인이었다.

관련토토 꽁머니 지급
- [허가/임상] 릭시아나 후발약 허가, BsAb 항암제 탈라타맙 3상 승인
- 닮은 꼴 동구토토 꽁머니 지급와 JW신약... 10년 새 매출 두 배 격차... 왜?
- 동구토토 꽁머니 지급제약, 전략적∙재무적 투자 통한 성과 창출 '눈길'
- [주간 제약] 동구토토 꽁머니 지급제약은 왜 조루 복합제 '구세정'을 출시할까
- 샌프란시스코로 향하는 K카지노 슬롯 머신 하는 법… 핫한 '비임상
- [허가/임상] 유행 지났는데... 발기부전 치료제 3품목 허가
- 동구토토 꽁머니 지급-씨티씨의 '조루+발기부전' 한 알... '새 시장' 만들까?
- 새해에도 간다, K카지노 엘에이, JP모건 헬스케어 콘퍼런스 총출동
- DongKoo Bio & CTC's 'Premature Ejaculation + ED' Pill: A New Market Forming?
- 굳센 동구·CTC 원투펀치, 허가는 '조루' 판매는 '발기부전'?
- 씨티씨토토 꽁머니 지급, 조루복합제 '원투정' 대만시장 진출 예고
- 새해에도 간다, K카지노 한국인, JP모건 헬스케어 콘퍼런스 총출동
- 이중특이항체 '임델트라', 소세포폐암 치료제로 허가

