베포타스틴베실산염 성분 항히스타민제도 8품목 동시 허가
인트라셀룰라 테라피스, 조울증 치료제 '카플리타' 3상 승인

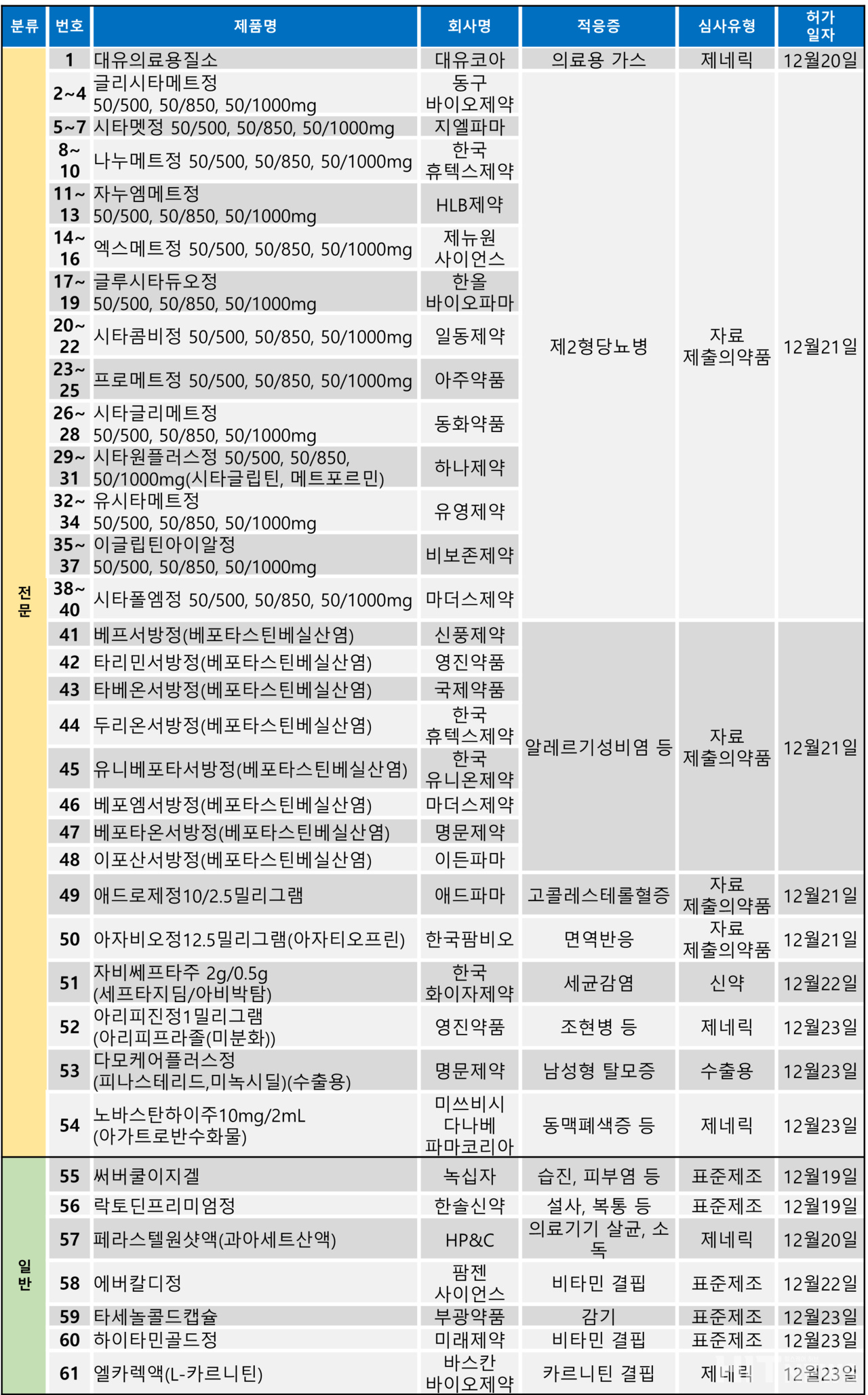
시타글립틴과 메트포르민 성분 제2형당뇨병 복합제가 대거 허가됐다.지난 주(12월 19일~12월 25일)에는 총 61개 품목이 식품의약품안전처로부터 품목허가를 받았다. 이 중 전문의약품은 54건, 일반의약품은 7건이었다.
이 전문의약품들은 시타글립틴염산염수화물과 메트포르민염산염 성분 제2형당뇨병 복합제가 39품목으로 주를 이뤘으며, 베포타스틴베실산염 성분 항히스타민제도 8품목이 허가됐다.
시타글립틴 성분은 DPP-4 억제제 계열 성분 제2형당뇨병 치료제로 이 성분과 메트포르민 복합제로는 한국엠에스디의 '자누메트'가대표적이다.
품목허가 업체는 △동구바이오사설 바카라 △지엘파마 △한국휴텍스사설 바카라 △HLB사설 바카라 △제뉴원사이언스 △한올바이오파마 △일동사설 바카라 △아주약품 △동화약품 △하나사설 바카라 △유영사설 바카라 △비보존사설 바카라 △마더스사설 바카라 등 13개로, 업체 모두 50/500mg, 50/850mg, 50/1000mg(메트포르민/시타글립틴) 등 3개 품목을 허가받았다.
대상 제제들의 위탁제조는 신일사설 바카라 충주 제1공장에서 맡아 진행할 예정이다.
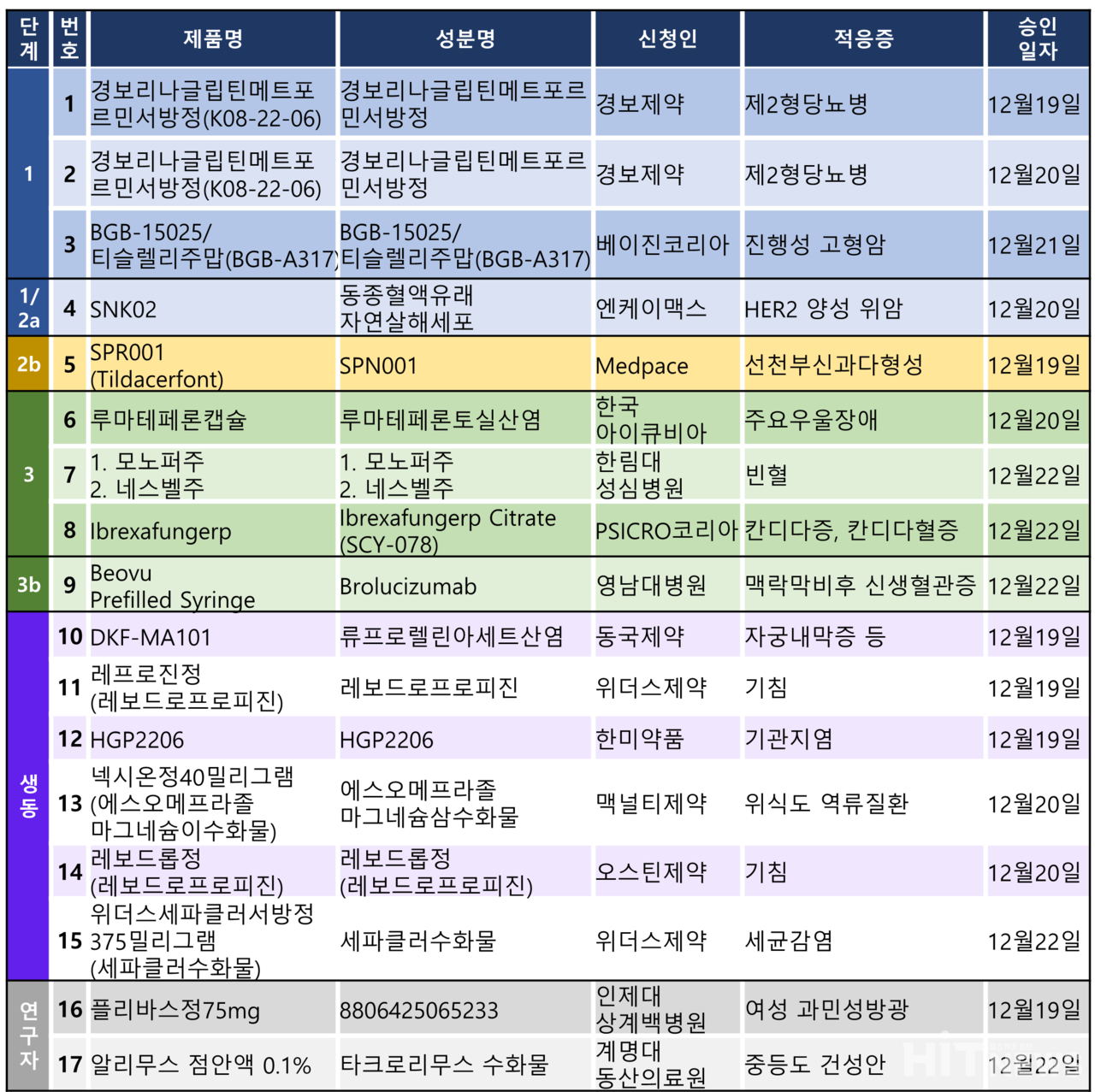
지난주 임상시험계획은 총 17건이 승인 완료됐다. 세부적으로 △1상 3건 △1/2a상 1건 △2b상 1건 △3상 3건 △3b상 1건 △생물학적동등성 6건 △연구자임상 2건 등이다.
이 임상시험들은 제2형당뇨병, 고형암, 위암, 주요우울장애 등 다양한 적응증에 대해 승인됐다.
미국 신약 개발사인 인트라셀룰라 테라피스(Intra-Cellular Therapies)의 조울증 치료제 '카플리타(성분명 : 루마테페론토실산염)'의 임상 3상 시험계획이 지난 20일 승인됐다.
이번에 시행되는 임상은 '주요우울장애 환자의 치료에서 부가요법으로서 루마테페론의 유효성 및 안전성을 평가하기 위한 무작위배정, 이중눈가림, 위약대조 다기관 임상시험'으로서 승인됐다.
이번 임상은 △노원을지대학교병원 △서울대학교병원 △삼성서울병원과 △전남대학교병원 △고려대학교의과대학부속안산병원 등 기관에서 진행될 예정이며, CRO는 한국아이큐비아가 맡았다.
카플리타는 미국 FDA로부터 2019년 12월 조현병, 지난해 12월 23일에는 조울증(양극성 장애) 치료제로 허가된 바 있다.
회사 측에 따르면, 이 약물은 세로토닌, 도파민 등 신경전달물질인 수용체에 대한 길항제로 작용해 주요우울증상을 억제하는 메커니즘을 가진다.

