백혈병·신경주위종·다발성골수종 환자들에 새 선택지 제공 예상
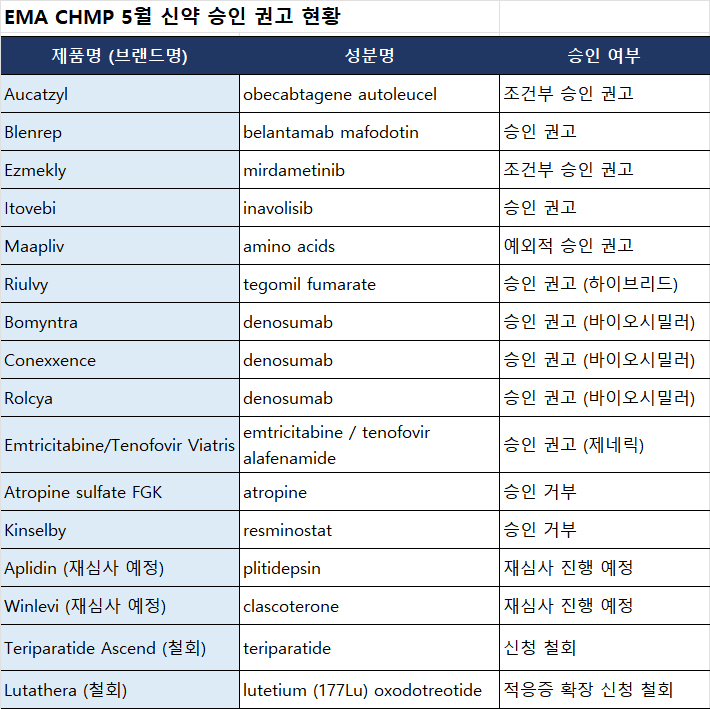
유럽의약품청(EMA)의 의약품위원회(CHMP)는 지난5월 정례회의에서 총 10개의 신약에 대해 판매 바카라 사이트 디시을 권고했다. 이번 바카라 사이트 디시 권고는 암, 희귀 유전질환, 신경계 질환 등 다양한 분야에 걸쳐 있으며, 이 중 일부는 조건부 바카라 사이트 디시 또는 예외적 바카라 사이트 디시의 형태로 진행됐다.
CHMP에 따르면 조건부 판매 바카라 사이트 디시을 받은 대표적인 치료제로는 'Aucatzyl(오베카브타젠 오토류셀)'이 있다. 재발성 또는 난치성 B세포 전구 급성 림프구성 백혈병 치료제로, EMA의 PRIME 프로그램의 지원을 받은 약물이다. PRIME은 치료 대안이 부족한 중대한 질환에 대해 개발과 바카라 사이트 디시을 신속하게 돕는 제도다.
또 다른 조건부 바카라 사이트 디시 권고를 받은 'Ezmekly(미르다메티닙)'는 1형 신경섬유종증 환자에게 나타나는 신경주위종(Plexiform neurofibroma) 치료를 위한 약물로, 소아 및 성인 모두를 대상으로 한다.
양성 의견을 받은 'Blenrep(벨란타맙 마포도틴)'은 60세 이상 성인에게 흔한 희귀 혈액암인 재발성 또는 난치성 다발성 골수종 치료제로, 치료 옵션이 제한적인 환자들에게 새로운 선택지를 제공할 전망이다.
유방암 분야에서는 'Itovebi(이나볼리십)'가 바카라 사이트 디시을 권고받았다. 이 약은 PIK3CA 돌연변이를 가진, 에스트로겐 수용체 양성(ER+), HER2 음성의 국소 진행성 또는 전이성 유방암 환자에게 사용된다.
희귀 유전질환인 단풍당뇨병(maple syrup urine disease) 치료를 위해 'Maapliv(아미노산 제제)'가 예외적 상황 하에서 바카라 사이트 디시 권고를 받았다. 이 질환은 단백질 내 특정 아미노산을 분해하지 못해 독성 물질이 체내에 축적되는 희귀병이다.
다발성 경화증(MS) 치료를 위한 'Riulvy(테고밀 푸마레이트)'는 13세 이상 청소년 및 성인 대상의 재발성 완화형 MS 치료제로 권고됐으며, 기존 의약품의 데이터에 의존한 하이브리드 신청 방식으로 제출됐다.
이번 회의에서는 골질환 치료를 위한 생물의약품 유사체(바이오시밀러) 3종도 바카라 사이트 디시 권고를 받았다. Bomyntra, Conexxence, Rolcya 모두 데노수맙 성분 기반으로 골다공증 및 골종양 예방·치료에 사용된다.
이와 함께, HIV-1 감염 치료를 위한 제네릭 의약품 Emtricitabine/Tenofovir alafenamide Viatris도 바카라 사이트 디시 권고를 받았다.
반면, 두 개의 약물은 바카라 사이트 디시 거부 의견을 받았다. Atropine sulfate FGK는 소아 근시 치료제로 사용될 예정이었으나, 3세 이상 어린이를 대상으로 한 적절한 효과 근거가 부족하다는 이유로 부정적 의견을 받았다. 또 다른 거부 사례인 'Kinselby(레스미노스타트)'는 피부에 주로 영향을 주는 혈액암인 진행성 균상식육종 및 세자리 증후군 환자 대상으로 제출됐지만, 효과성에 대한 의문으로 바카라 사이트 디시되지 않았다.
또한, 이미 바카라 사이트 디시된 네 가지 의약품(Imfinzi, Rezolsta, Saxenda, Tevimbra)에 대해서는 적응증 확대가 권고됐다.
재심사 관련해선, 2017년 부정적 의견을 받았던 'Aplidin(플리티뎁신)'에 대해 유럽연합집행위원회가 거부 결정을 철회하면서 EMA가 재심사를 시작하게 됐고, 2025년 4월 회의에서 부정적 의견을 받은 여드름 치료제 Winlevi(클라스코테론) 역시 재심사가 요청된 상태다.
한편, 골다공증 치료제로 신청된 Teriparatide Ascend와 소화계 신경내분비종양 치료제로 적응증 확장을 시도했던 Lutathera는 각각 신청이 철회됐다.
오랜 기간 다양한 감염병 치료에 사용되어온 항생제 아지트로마이신에 대해 CHMP는 일부 적응증의 변경 및 삭제를 포함한 사용 최적화 권고를 내렸다.
